Depois de a Moderna anunciar a intenção de distribuir a vacina contra a Covid-19 Spikevax na América Latina, a Anvisa (Agência Nacional de Vigilância Sanitária) se debruça sobre a concessão de licença para uso do imunizante no país. Nesta segunda-feira, a reguladora reuniu-se com representantes da farmacêutica e da empresa parceira Zodiac Produtos Farmacêuticos para tratar sobre a regularização da vacina.
"Foram discutidas as possibilidades de solicitação de autorização de uso emergencial, bem como registro no Brasil para a vacina contra a Covid-19", detalhou, em nota, a Anvisa, que escalou integrantes da Gerência-Geral de Medicamentos e Produtos Biológicos para participar do encontro.
Agora, a Moderna precisa protocolar o pedido. A indicação é que o pleito seja pelo registro definitivo, uma vez que o anunciado fim do estado de emergência em saúde pública pode colocar em xeque o uso de imunizantes em caráter emergencial. É o caso da Coronavac.
A vacina Spikevax foi desenvolvida com base na plataforma de RNA mensageiro, mesma tecnologia usada pela Pfizer, que possui registro definitivo no Brasil e está incluida no PNO (Plano Nacional de Operacionalização da Vacinação contra a Covid-19).
A Moderna anunciou, em março, a distribuição da Spikevax em 18 países latino-americanos, entre eles o Brasil. A vacina já foi autorizada para uso em mais de 80 países e possui registro definitivo nos Estados Unidos, além de autorização emergencial da OMS (Organização Mundial da Saúde).
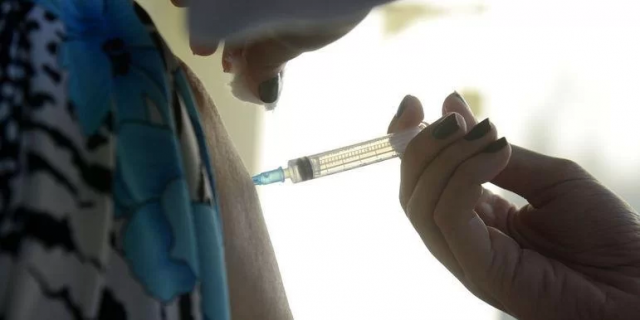
Uso da vacina da Moderna será analisado pela Anvisa | Foto: Tomaz Silva / Agência Brasil


